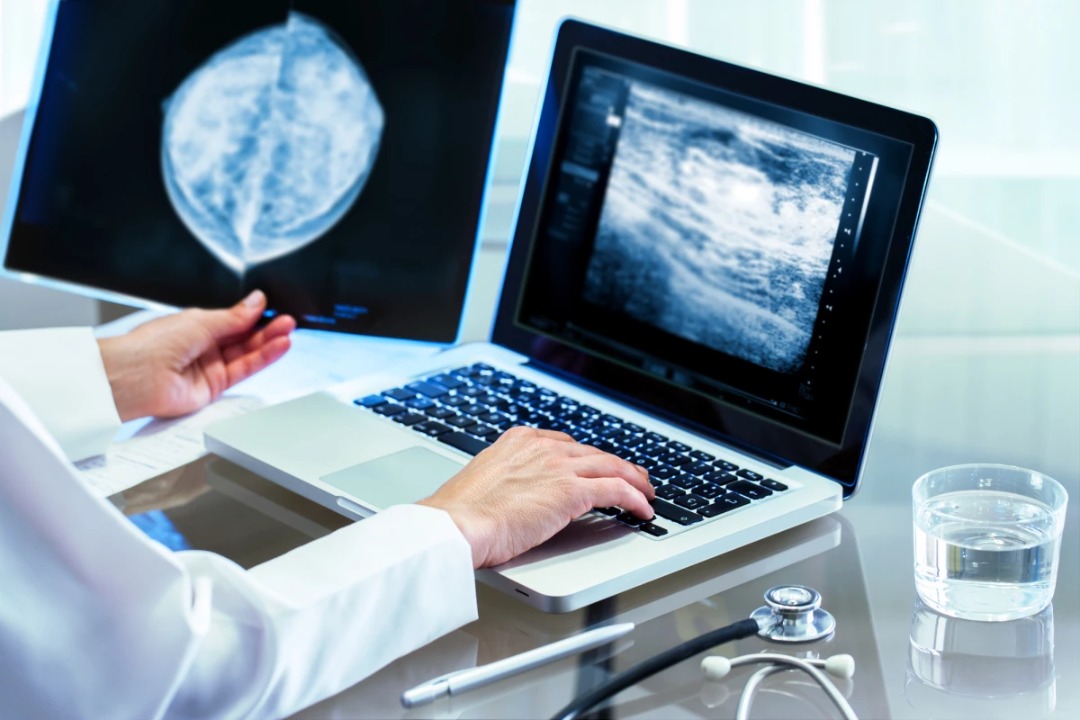
تصویب دو روش درمانی جدید سرطان سینه
ایسنا علوم پزشکی تهران – سازمان غذا و داروی ایالات متحده (FDA) دو نوع جدید از درمان سرطان سینه را تصویب کرده است ، یکی سرطانهای مثبت با HER2 و دیگری برای سرطان پستان سه گانه منفی متاستاتیک....
ایسنا علوم پزشکی تهران – سازمان غذا و داروی ایالات متحده (FDA) دو نوع جدید از درمان سرطان سینه را تصویب کرده است ، یکی سرطانهای مثبت با HER2 و دیگری برای سرطان پستان سه گانه منفی متاستاتیک. صدور تأییدیه FDA برای هر دو روش درمانی به دلیل بیماری همه گیر کروناویروس تسریع شد.
به گزارش ایسنا علوم پزشکی تهران به نقل از اطلس نیوز، به عنوان بخشی از تعهد مداوم و تهاجمی سازمان غذا و داروی ایالات متحده برای پرداختن به بیماری همه گیر کروناویروس ، آنها اعلام کردند ما همچنان تمرکز خود را بر بیماران مبتلا به سرطان که جمعیت آسیب پذیر در معرض خطر ابتلا به این بیماری را تشکیل می دهند ، حفظ می کنیم. در این زمان بحرانی ، این سازمان همچنان به تسریع روند توسعه محصولات انکولوژی می پردازد.
در ۱۷ آوریل FDA با استفاده از مجوز درمانی داروی جدید به نام توکیسا (tucatinib) را تصویب کرد. تصویب این امر برای استفاده از توکیسا در ترکیب با شیمی درمانی برای بیمارانی است که مبتلا به سرطان پستان متاستاتیک HER2 مثبت هستند.
این تأییدیه برای توکیسا به عنوان یک روش دست اول نیست. در عوض ، بیماران قبل از شروع توکیسا حداقل باید یک دوره درمان ضد HER2 قبلی داشته باشند.
این تأییدیه براساس داده های کارآزمایی بالینی فاز سه که اخیراً منتشر شده نشان می دهد که نتایج مثبتی از درمان ترکیبی جدید دارد. این روش به ویژه ، امیدواری را در بیمارانی که متاستاز مغزی دارند به وجود آورده ، شکل تهاجمی از این بیماری که احتمال زنده ماندن بیماران در آن بسیار کم است.
توکیسا چهار ماه قبل از تاریخ مشخص شده توسط FDA تأیید شد ، این نمونه ای از این تعهد را نشان داد و اینکه چگونه کار منظم در بررسی درمان مبتلایان به سرطان بدون تأخیر پیش می رود.
در ۲۲ آوریل سازمان غذا و داروی ایالات متحده تصویب سریع را به Trodelvy اعطا کرد. این روش درمانی برای بیمارانی است که دارای شکلی خاص از سرطان پستان ، معروف به سرطان سینه منفی سه گانه هستند.
داروی ترادلوی با مجموعه ای نسبتاً شدید از عوارض جانبی احتمالی همراه است ، بنابراین تأییدیه FDA فقط اجازه می دهد تا در صورت عدم موفقیت حداقل دو روش درمانی دیگر ، این روش درمانی بر روی بیماران انجام شود.
مجوز برنامه ترادلوی نیز فقط تحت شرط “تأییدیه شتاب” اعطا شد. این بدان معناست که آزمایشات بالینی یا داده های بالینی قبل از تأیید کامل این دارو لازم خواهد بود.
شیمی درمانی اصلی ترین درمان برای سرطان سینه منفی سه گانه است. تصویب مجوز داروی ترادلوی نوید بخش یک روش درمانی جدید برای بیماران مبتلا به تومور بدخیم است.
مانند پرونده توکیسا ، صدور تاییدیه Trodelvy به دلیل تعهد سازمان غذا و دارو در ارائه پر شتاب درمانهای انکولوژی در طول همه گیری کووید-۱۹ تسریع شد.
مترجم: مجید پوست چیان





هیچ نظر! یکی از اولین.